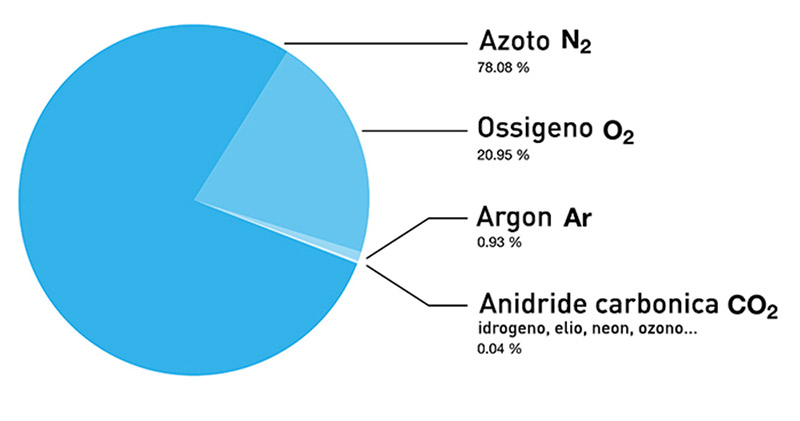
L’azote est tiré directement de l’air que nous respirons chaque jour, composée de 78% d’azote, de 21% d’oxygène, de petites quantités de dioxyde de carbone, d’hydrogène, d’hélium, de gaz rares (argon, crypton, néon et xénon), de vapeur d’eau et de polluants.
QU’EST-CE QUE L’AZOTE
HISTORIQUE
L’azote a été découvert vers la fin du 1700. Jusqu’au début du XIXe siècle, les scientifiques croyaient que l’air et ses composants principaux, l’azote et l’oxygène, étaient « gaz permanents » et ne pouvaient jamais être réduits à l’état liquide. Ce n’est qu’en 1877 que Louis Cailletet en France et Raoul Pictet en Suisse ont produits dans leurs laboratoires des gouttes bleutées d’air liquide. Ensuite, vers la fin du siècle, l’allemand Karl Von Linde et le français Georges Claude ont découvert, indépendamment l’un de l’autre, des techniques pour produire de l’air liquide et en séparer les composants gazeux à une échelle industrielle.
Les deux techniques étaient basées sur les mêmes 3 principes:
La température de liquéfaction d’un gaz change selon la pression exercée sur celui-ci;
Les gaz chauffent quand ils sont comprimés et ils refroidissent quand ils s’étendent. Cela peut être constaté à travers l’observation d’une capsule de dioxyde de carbone qui transforme l’eau commune en eau gazeuse : le gaz est comprimé dans la capsule à une pression quatre ou cinq fois plus élevée que celle dans l’atmosphère et, une fois le gaz libéré dans l’eau de la bouteille, la capsule s’avère glacial au toucher;
Il est possible de séparer un liquide de ses composants gazeux à travers l’ébullition. La partie la plus volatile s’élèvera comme vapeur et pourra être refroidie et condensée pour être restaurée à l’état liquide dans un autre récipient. C’est le même processus qui suit un agriculteur qui distille l’alcool du jus fermenté du fruit lors de la préparation du brandy de pomme. La différence entre cette opération et le travail d’une installation pour la séparation de l’air ne concerne que la température : le point d’ébullition des gaz de l’air à la pression atmosphérique, qui représente également le point dans lequel ils deviennent liquides, est -183 °C pour l’oxygène et -196°C pour l’azote, donc très bas. Pour arriver à ces températures, la technique a dû faire des merveilles.

Louis Cailletet

Raoul Pictet

Karl Von Linde
Le processus dans une installation pour la séparation de l’air commence quand des compresseurs énormes aspirent l’air extérieur et la filtrent de la vapeur d’eau, du dioxyde de carbone et des polluants. Une fois purifiée, l’air est soumis à grande pression (jusqu’à 20 fois plus élevée que celle de l’atmosphère) pour pouvoir ensuite être étendue et utilisée comme réfrigérant. Comme la pression en augmente de manière drastique la température, l’air est mis en circulation à travers des unités réfrigérantes et soumis à traitements ultérieures pour pouvoir arriver à -80°C : à ce point du processus, la pression sur la quasi-totalité de l’air est six fois moindre que la norme.
Comme conséquence de l’expansion, cette masse d’air refroidit le reste, qui continue d’être soumis à haute pression, jusqu’à -160°C. Il commence en ce moment la formation d’un liquide bleuté appelé air liquide, ensuite canalisé dans un dédale de tubes et d’échangeurs, de pressions qui expandent et contractent, de températures qui montent et baissent, jusqu’au point de distillation : on élimine l’azote à travers l’ébullition pour enfin obtenir de l’oxygène pur.

La distillation a lieu dans des colonnes en acier inoxydable dans lesquelles des centaines de plateaux sont entassés, chacun perforé de milliers de trous minuscules. Le gaz monte à travers les trous pendant que le liquide, en débordant des plateaux, se verse dans le niveau au-dessous. Ainsi, le gaz s’enrichit d’azote et le liquide d’oxygène. Ce processus est invisible, tout comme beaucoup d’autres dans cette industrie.
Comme elles doivent être accomplies à des températures si basses, les opérations ont lieu dans les parois métalliques de ce qu’on appelle une boite froide (cold-box), de laquelle il peut sortir de l’azote à l’état liquide ou gazeux en fonction d’où et de comment il doit ensuite être livré.
L’azote peut être transporté sous pression dans des grands réservoirs et ensuite stocké à l’état liquide sous pression ou à pression atmosphérique dans de spéciaux réservoirs isolés aussi dits «Dewar ». L’isolation de ces réservoirs, en minimisant le flux de chaleur vers l’intérieur du réservoir, réduit la perte d’azote due à l’évaporation du liquide : avec ce système l’azote liquide (-195,82 °C) peut être utilisé comme un puissant réfrigérant.
Afin d’obtenir des températures inférieures il est normalement nécessaire l’utilisation d’hélium liquide (-268,9 °C).
